本文來自格隆匯專欄:醫藥魔方,作者:Cassie
在美國,每10張處方就有9張使用仿製藥。仿製藥佔90%處方,但其支出僅佔總處方額的20%。
美國是全球最重要的醫藥市場之一,也是全球最大的仿製藥市場。根據AMM2020年年度報吿,在美國,每10張處方就有9張使用仿製藥。仿製藥佔90%處方,但其支出僅佔總處方額的20%。在過去十年裏,仿製藥為美國民眾和醫療系統接近省下2.2萬億美元。即便如此,仿製藥依舊佔美國短缺藥物榜首。
“如果買不起,即使是世界上最好的藥品也無濟於事”。如果説創新藥能夠滿足未被滿足的臨牀需求,仿製藥則大大提高了藥物的可及性與可負擔性。創新與仿製本就沒有高低之分,甚至可以説,偽創新還不如高質量的仿製。創新總是先行於仿製,有必要授予專利保護補償創新;仿製藥可以平抑藥價,減輕患者的用藥經濟負擔,同樣有必要激勵仿製。
因此,創設藥品專利鏈接制度,有助於增強制藥行業的競爭,平衡創新與仿製的利益,促進創新藥與仿製藥共同發展。
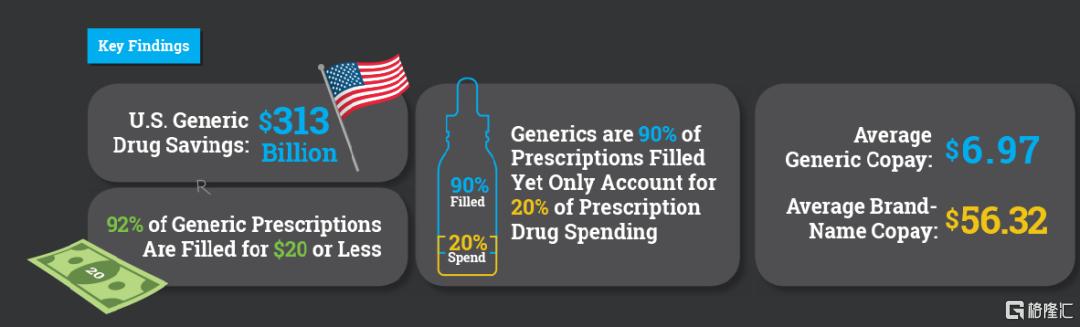 美國仿製藥處方佔比 (來源:2020 AAM Generic Drug & Biosimilars Access & Savings Report)
美國仿製藥處方佔比 (來源:2020 AAM Generic Drug & Biosimilars Access & Savings Report)
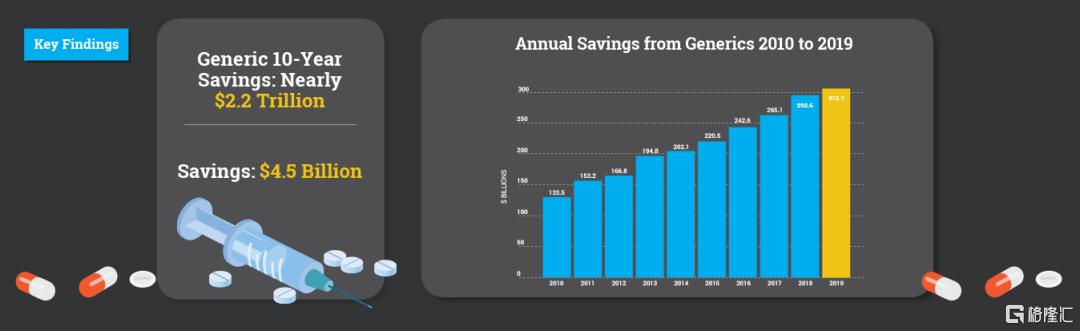
2010-2019年美國仿製藥節省資金一覽(來源:2020 AAM Generic Drug & Biosimilars Access & Savings Report)
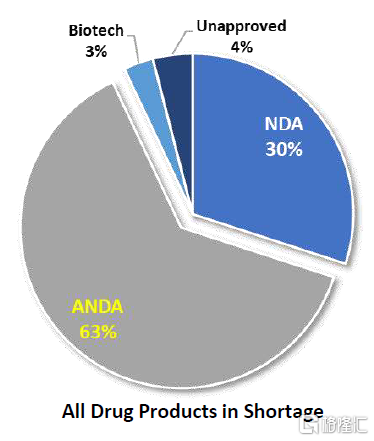
美國最新藥物短缺分佈比例(來源:GDF 2021 Generic Drugs Forum)
制度沿革:曲折前行的美國藥品監管史
美國食品藥品監督管理局FDA被視為全球藥品監督管理的標杆,FDA的發展歷程,也是藥品監督管理不斷規範完善的歷程。但歷史吿訴我們,事物得到發展前必然經過血淋淋的教訓。
經歷了上世紀著名兩大“藥害”事件—磺胺酏劑和“反應停”事件後,美國先後通過了《Food & Drug Act》和《Kefauver-Harris Amendment》,前者規定新藥必須被證明安全才可以上市銷售,後者規定了任何藥物在上市之前除了需要被證明是安全的,還必須是有效的。FDA以“零風險控制”為理念,對新藥研發和生產的每個環節進行嚴格監控。該法案的實施在很大程度上確保了新藥的安全性與有效性,避免藥害事件再次發生。
Kefauver-Harris法案在很長時間裏主導着美國的新藥審批進程,但其繁宂的監管審批流程不僅延緩新藥上市步伐,還同時增加了創新藥和仿製藥生產商的研發負擔。該法案對創新藥和仿製藥審批“一視同仁”,即創新藥與仿製藥均要通過相同的安全性和有效性試驗才能獲批上市。一方面,創新藥生產商必須要進行大規模臨牀安全性和有效性試驗,由於研發環節佔用太多時間,導致新藥上市後的專利保護期大幅縮短,創新藥收入鋭減,創新藥生產商研發積極性不高;另一方面,仿製藥被要求對已經被證明安全和有效的創新藥,進行同樣的安全性和有效性試驗,消減了仿製藥企的積極性,束縛了仿製藥行業的發展。再者,由於仿製藥上市滯後,新藥得以壟斷市場,藥價居高不下,創新藥企也失去了研發新藥的危機感,加深了患者的經濟負擔和政府的醫療保健成本,由此陷入的惡性循環給患者、製藥廠商和監管當局均帶來不利影響。
為了平衡創新藥生產商和仿製藥生產商的利益,1984 年,美國通過了《Hatch-Waxman Amendment》,又名《Drug Price Competition and Patent Restoration Act》(藥品價格競爭與專利期補償法案)。該法案由美國眾議員Hatch和參議員Waxman提出,因此以兩人名字命名。
Hatch-Waxman法案首次確立仿製藥的審批途徑,即申請人可以根據聯邦食品、藥品和化粧品法案(FD&C法案)下的505(j)遞交簡略新藥申請(Abbreviated New Drug Application,ANDA)。仿製藥廠商在向FDA提出ANDA時,無需再進行藥物安全性、有效性等研究,僅需提供生物有效性(Bioequivalence)的試驗結果。另外,在仿製藥廠商準備ANDA期間,法案還給予其專利侵權的豁免,使專利到期之前仿製藥廠商便可開始仿製藥的研製,保證在藥物專利期屆滿後仿製藥及時上市。在保護新藥研發方面,法案規定FDA會給予新藥適當的數據獨佔保護。此外,對於新藥行政審批過程中耽擱的時間,原研藥廠商也能獲得相應的專利保護期補償。Hatch-Waxman法案同樣涉及新藥申請相關的的專利和獨佔期(Patents and Exclusivities)條款,以及某些 ANDA 申請的 180天獨佔期。這部法案是藥品專利鏈接制度的起源,一方面有效保護了新藥的專利權,另一方面提升了美國仿製藥的市場競爭力。
藥品專利鏈接制度:創新與仿製的利益制衡
藥品專利鏈接制度(Pharmaceutical Patent Linkage system)是指仿製藥上市批准與創新藥品專利期滿相“鏈接”,即仿製藥註冊申請應當考慮先前已上市藥品的專利狀況,從而避免可能的專利侵權。
該制度有兩層含義:一是美國FDA與美國專利商標局(USPTO)的職能鏈接,即從鼓勵藥物創新的角度,授予創新藥專利保護期延長以充分保護;二是仿製藥的上市申請審批與相應的藥品專利有效性審核的程序鏈接,即鼓勵仿製藥利用規則,通過專利挑戰以及專利規避儘快合法地提前上市,提高藥品的可及性和可負擔性。
美國的藥品專利鏈接制度主要包括以下五方面內容:
(一)藥品專利保護期延長
製藥企業在進行新藥開發時,一般只要完成新藥的單體篩選,就可以申請專利保護。由於一款新藥需要經過漫長的開發和審批時期才迎來最終上市,而新藥獲批上市時的專利期往往只剩一半,所剩期限不足以讓原研藥企收回新藥研發的支出。為了調動原研藥企的研發積極性,Hatch-Waxman法案規定,權利人可以就產品專利、用法專利或者製造方法專利中選擇其中一種來延長保護期限,但是延長專利期的藥品必須滿足一定條件,即產品專利尚未到期;專利沒有經過延期;產品必須是經過 FDA 審批並取得上市許可的。
事實上,藥品專利的延長包括專利期調整(Patent Term Adjustment,PTA)和專利期延長(Patent Term Extension)。PTA為因USPTO審查延誤而給予的補償;PTE為針對臨牀試驗和新藥行政審批的補償,PTE延長時間最多不超過5年,延長期限加上藥物上市時所剩餘的專利期限之和不能超過14年。但如果是由於申請人未盡到應有的注意義務而導致專利期耽擱的,該期間將不計入延長期內,且同一藥物只能申請一次專利期間延長。
(二)Bolar例外(Bolar exception)
Bolar例外源於Bolar v.羅氏(Roche)一案,具體指“單純旨在獲得和提交FDA 審批時需提交的信息,而在美國製造、銷售、許諾銷售或者向美國進口專利藥品或專利醫療器械的行為不構成侵犯專利權行為”。該條款為仿製藥在新藥專利期屆滿前儘快獲得上市審批所需的數據提供了法律依據,縮短了仿製藥上市的時間,既激發了仿製藥公司的積極性,也削減了新藥在專利期屆滿後享有的實質性壟斷,促進了仿製藥的發展。
(三)市場獨佔期(Market Exclusivity)
Hatch-Waxman法案授予新藥上市申請人一定時期的試驗數據獨佔權。試驗數據是指創新藥企申請新藥上市時向藥品監管機構遞交的能證明該藥品有效性和安全性的一系列數據。在數據獨佔期內,哪怕專利已過期,原研藥企仍然可以單獨佔領市場,FDA不再受理相同的仿製藥上市申請,但仿製藥申請人自行取得的試驗數據除外。獨佔期限根據藥品類型的不同而異,其中,最主要的是新藥的數據獨佔。根據獨佔期類型的不同,獨佔期分為:

獨佔期 來源:FDA 整理:Cassie
(四)橙皮書(Orange Book)
由FDA出版並定期修改的《經治療等同性評價標準的藥品》(Approved Drug Products with Therapeutic Equivalence Evaluation),因其封皮是橙色,也被稱為“橙皮書”。該書詳細完整地列出了FDA批准上市的所有藥品,以及這些藥品涉及的專利和獨佔期信息。根據Hatch-Waxman法案,原研藥企向FDA遞交新藥上市許可申請(New Drug Application,NDA)時,需同時提供該藥物相關的專利信息。當NDA申請獲批後,對應的專利就會被收錄到橙皮書中,為日後仿製藥企開發仿製藥、提交ANDA、或設計專利迴避等提供參考。FDA規定可以列入橙皮書的專利包括:活性化合物、配方、組合物、藥物用途;不能列入橙皮書的專利包括:製造工藝、外包裝、代謝物、中間體等。當專利無效或過期,又或是市場獨佔期到期,藥物專利將從橙皮書中剔除。
(五)仿製藥簡化申請(Abbreviated New Drug Application, ANDA)
為簡化仿製藥上市程序,加快仿製藥上市進程,Hatch-Waxman進一步設立仿製藥上市申請ANDA路徑。即仿製藥申請人申請仿製藥上市時,無需重複進行已經證明的安全性和有效性研究,只需以新藥為參照標準進行相應的生物等效性研究,證明該仿製藥與原研藥具有相同的活性成分、生產規程、劑型、強度和生物有效性即可。仿製藥可以在原研藥專利過期之前以研究目的進行樣品生產,但不可以進行商品生產。此外,為避免專利侵權,促進仿製藥合規上市,還規定仿製藥在申請時必須作專利聲明,聲明分別如下:

專利聲明 來源:文獻[1]
對於作出第I段和第II段聲明的ANDA,FDA 可以直接批准該ANDA;以第III段聲明申請的ANDA,在相關專利期屆滿後方可批准;採用第IV段聲明的ANDA,會進入專利挑戰程序(圖4),仿製藥企必須在提出申請後的20天內通知原研藥企或相關專利持有人。原研藥企或相關專利持有人在收到通知的45天內有權向法院提出專利侵權訴訟,專利持有人若在這45天內提出專利侵權訴訟,FDA則會把仿製藥上市審批往後延遲30個月,但這期間FDA 對仿製藥的技術評審仍在繼續。專利持有人可以在這期間申明自己的專利權利,這30個月稱為“30個月遏制期”(30-month stay)。而第一個在 ANDA 申請中提交第IV類證明併成功挑戰專利的仿製藥,稱為“首仿藥”(first generic),首仿藥將擁有“180 天市場獨佔期”(180-day exclusivity),FDA在該期限內不會批准其他相同仿製藥的上市申請。
“180 天市場獨佔期”不但可以給仿製藥企帶來豐厚的收益,更激勵了仿製藥企向原研藥企發起專利挑戰,促進了仿製藥的發展。
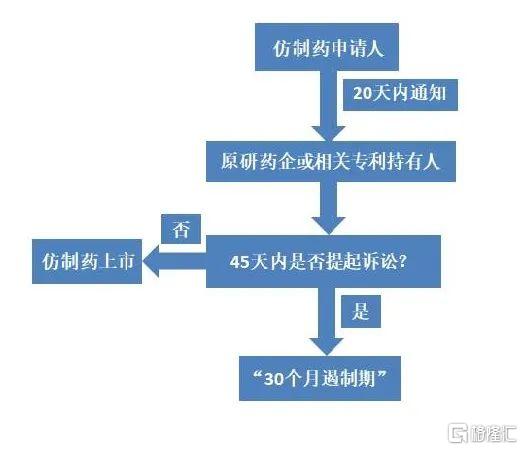
仿製藥專利挑戰流程 來源:文獻[1]
小結
Hatch-waxman法案開創性地建立了藥品專利鏈接制度,充分平衡了相關各方利益。對於創新藥,賦予其專利保護期延長、數據獨佔期、30月遏制期等權利,既能充分保護原研藥企的知識產權,又能鼓勵藥物創新。更重要的是,這部法案建立仿製藥ANDA申請途徑、發佈橙皮書、鼓勵仿製藥企挑戰專利獲得180天獨佔期等,有利於加快仿製藥上市步伐,提高仿製藥的市場競爭力,增加藥物的可及性和可負擔性。